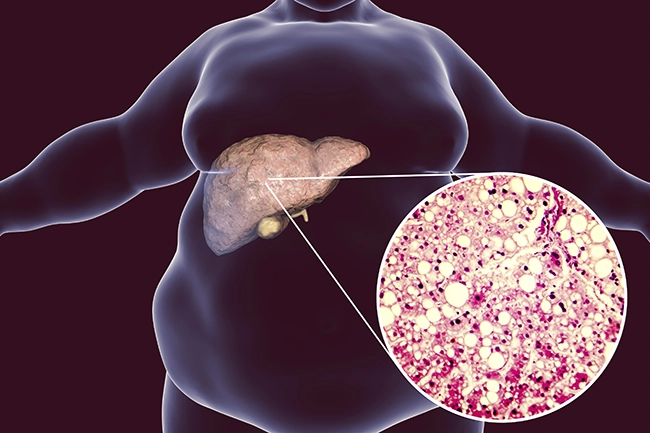
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печени или жировой гепатоз, неалкогольный стеатогепатит)
— это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
Все эти изменения неуклонно приводят к:
1. разрушению клеток печени (неалкогольный стеатогепатит);
2. накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
изменению биохимического состава крови;
3. развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
4. в конечном итоге, циррозу.
Продукция от компании Сово-Сова при жировом гепатозе.
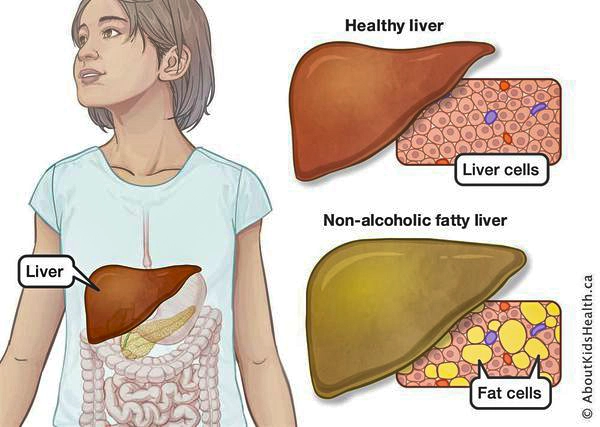
Структура здоровой печени и печени при НАЖБП
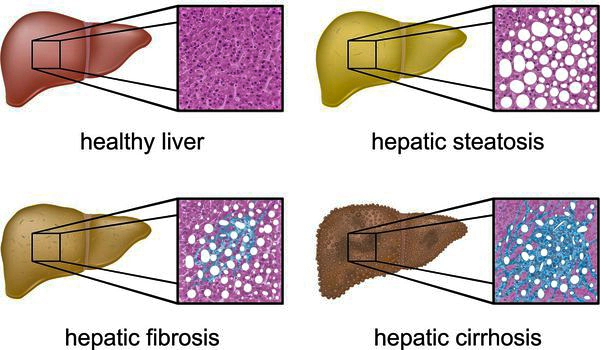
Патологические изменения ткани печени
Метаболический синдром
— широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией.
В большинстве случаев НАЖБП развивается после 30 лет.
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются:
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
- При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %.
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ):
ИМТ = вес (кг) : (рост (м))2.
Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3.
Этот результат говорит об ожирении I степени.
16 и менее — выраженный дефицит массы;
16-17,9 — недостаточная масса тела;
18-24,9 — нормальный вес;
25-29,9 — избыточная масса тела (предожирение);
30-34,9 — ожирение I степени;
35-39,9 — ожирение II степени;
40 и более — ожирение III степени (морбидное).
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
У 50-75% больных могут появляться симптомы общей (хронической) усталости, снижение работоспособности, недомогание, слабость, тяжесть в области правого подреберья, набор веса, длительное повышение температуры тела без всякой причины, красные точки на коже в области груди и живота. Печень часто увеличена. Возникают расстройства пищеварения, повышенное газообразование, кожный зуд, редко — желтуха, «печёночные знаки».
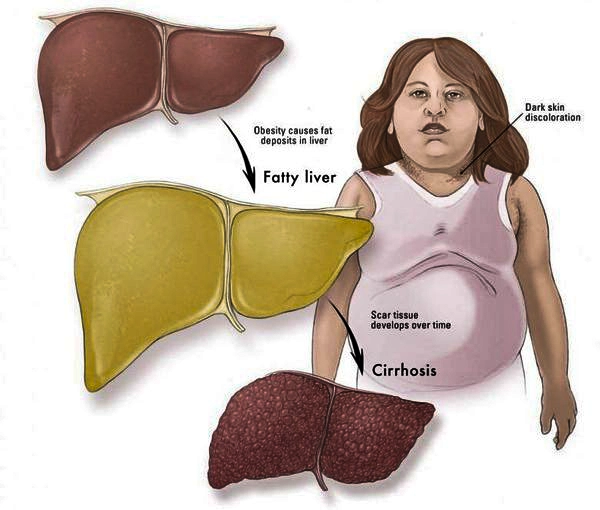
Признаки НАЖБП
Часто НАЖБП сопутствуют заболевания желчного пузыря:
хронический холецистит, желчнокаменная болезнь.
Реже, в запущенных случаях, возникают признаки портальной гипертензии:
увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости).
Как правило, данные симптомы наблюдаются на стадии цирроза печени.
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности.[7]
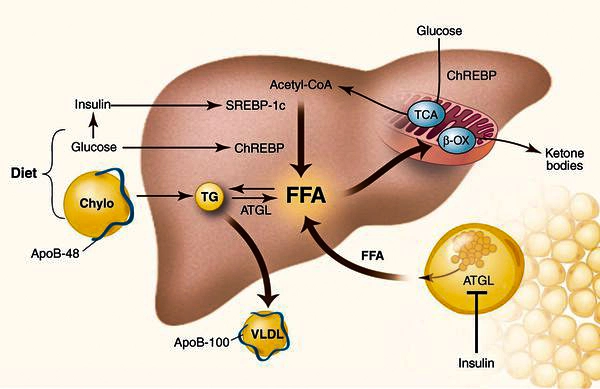
Механизм накопления холестерина в печени
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот,
что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны
и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид.
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной,
раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах,
в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
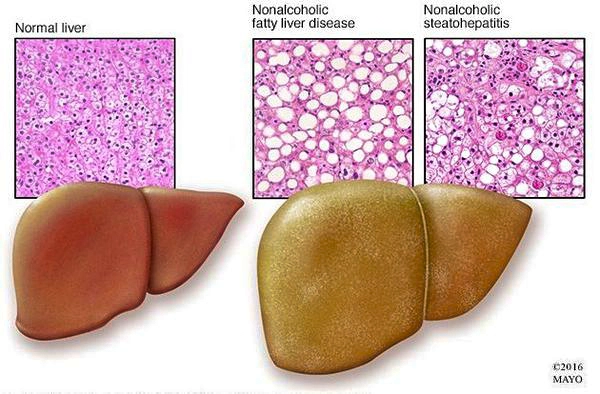
Увеличение гепатоцитов и нарушение функции печени
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов,
которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз.
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу , а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.
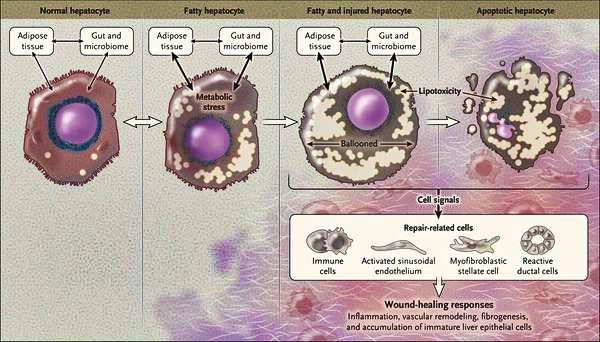
Некроз клеток печени
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt:
I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
S1 (до 33% жировой инфильтрации);
S2 ( 33-60% жировой инфильтрации)
S3 (более 60% жировой инфильтрации)
F1,F2, F3, цирроз.
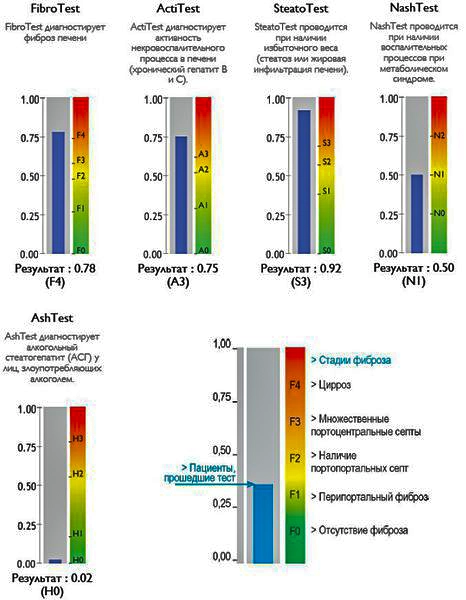
Степени выраженности жировой инфильтрации
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени
— гепатоцеллюлярную карциному. Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
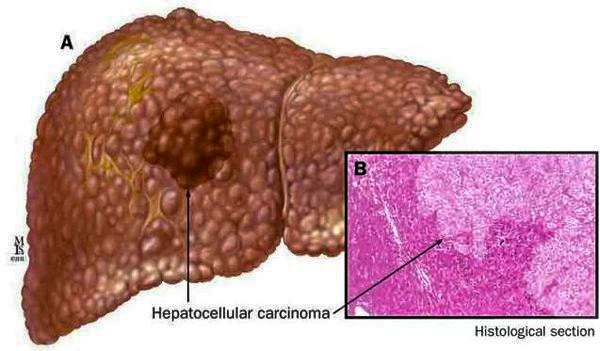
Гепатоцеллюлярная карцинома
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов.
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ, МСКТ, МРТ и эластометрии (FibroScan),
при необходимости исследуется морфологическое состояние — биопсия печени.
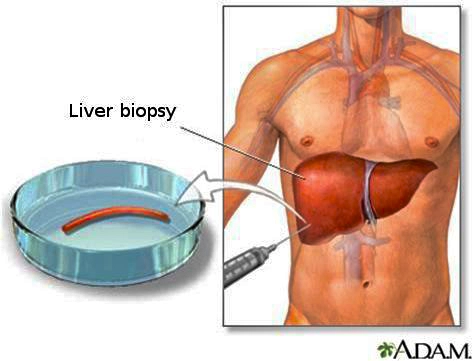
Биопсия печени
С помощью эластометрии исследуется эластичность мягких тканей.
Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового (НАЖБП) гепатоза, неалкогольной жировой болезни печени
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
Для предупреждения развития потенциально летальных осложнений (в том числе и со стороны сердечно-сосудистой системы) необходимо следующее:
- 1. Скрининг на НАЖБП для пациентов группы риска;
- 2. Своевременная постановка диагноза;
- 3. Своевременное проведение эффективной терапии препаратами с высоким профилем безопасности, воздействующими не только на гепатоцит, но и на патогенез развития сердечно-сосудистых осложнений.
Основной целью терапии является уменьшение выраженности стеатоза и предотвращение прогрессирования заболевания в стадии стеатогепатита, фиброза или цирроза, а также снижение риска сердечно-сосудистых осложнений.
Основные принципы лечения НАЖБП:
- 1. снижение массы тела (диета и физические нагрузки);
- 2. обязательная отмена потенциально гепатотоксичных лекарственных препаратов, кроме случаев, когда польза от их назначения превышает риск;
- 3. коррекция метаболических нарушений:
- a. повышение чувствительности клеточных рецепторов к инсулину (метформин, тиазолидиндионы);
- b. коррекция нарушений липидного обмена;
- c. гипотензивная терапия;
- 4. лечение окислительного стресса.
-
Снижение веса и физическая активность
Доказано, что у пациентов с НАЖБП комплексные меры по изменению образа жизни, приводящие к разрешению заболевания, способствуют снижению риска смерти от сердечно -сосудистых осложнений на 40%, что сопоставимо с эффективностью медикаментозной коррекции.
- – Пациентам с НАЖБП рекомендованы диетотерапия с постепенным снижением веса и увеличение физической нагрузки, они являются ведущими факторами в лечении НАЖБП. Потеря веса при использовании гипокалорийной диеты или ее сочетание с повышенной физической активностью способствует уменьшению проявлений стеатоза
- – Подбор диеты и выбор типа и объема физической нагрузки рекомендовано адаптировать к индивидуальным предпочтениям пациента
- – Пациентам с НАЖБП противопоказано злоупотребление алкоголем, на стадии ЦП рекомендовано воздерживаться от употребления алкоголя и табакокурения Фармакологическая коррекция инсулинорезистентностиДля лечения сопутствующего нарушения толерантности к углеводам и профилактики развития СД 2 типа пациентам с НАЖБП рекомендуется #метформин** в дозе из расчета 20 мг/кг веса пациента/сутки (общая суточная доза 1000-2000 мг, дозу наращивать постепенно, начиная с 500-850 мг/сут) курсами не менее года
Комментарии: В клинических исследованиях по изучению эффективности метформина показано снижение резистентности к инсулину, уменьшение активности трансаминаз и выраженное снижение веса (более 10 кг) у 19% пациентов с НАЖБП. Однако улучшение гистологической картины печени было незначительным: уменьшения выраженности стеатоза удается достигнуть только у 30% пациентов.
- – Метформин** не рекомендуется в качестве специфического средства для лечения НАЖБП с синдромом ИР, поскольку не оказывает существенного влияния на гистологическую структуру печени [2, 36].
Комментарии: Данные метаанализа показали, что применение метформина в течение 612 мес на фоне изменения образа жизни не снижает выраженности цитолиза, но улучшает гистологическую структуру печени аналогично контрольной группе, не принимавшей препарат, но изменявшей образ жизни [35].
#Пиоглитазон
- – #Пиоглитазон в дозе 30 мг в сутки рекомендован как препарат выбора для лечения морфологически подтвержденного НАСГ у пациентов с СД2, однако его безопасность и эффективность при длительной терапии не доказана [35, 36].
Комментарии: Пероральное гипогликемическое средство, селективный агонист гамма-рецепторов (PPAR-гамма), обнаруживаемых в жировой, мышечной тканях и в печени. Активация ядерных рецепторов PPAR-гамма модулирует транскрипцию ряда генов, чувствительных к инсулину, участвующих в контроле уровня глюкозы и в метаболизме липидов. Пиоглитазон снижает инсулинорезистентность в периферических тканях и в печени, в результате этого происходит увеличение расхода инсулинозависимой глюкозы и уменьшение продукции глюкозы в печени.
При СД2 уменьшение инсулинорезистентности под действием пиоглитазона приводит к снижению концентрации глюкозы в крови, снижению уровня инсулина в плазме и гемоглобине A1c (гликированный гемоглобин, HbA1c), снижению уровня ТГ и увеличению уровня ЛПВП, однако уровень ЛПНП и общего холестерина у таких пациентов не изменяется.
Фармакологическая коррекция гиперлипидемии
Гиполипидемическую терапию следует проводить с учетом стадии НАЖБП, при необходимости – в комбинации с лекарственными препаратами, оказывающими гепатопротекторное действие. Наиболее распространенными и изученными гиполипидемическими препаратами являются ингибиторы ГМК-КоА редуктазы.
- – У пациентов с НАЖБП ингибиторы ГМК-КоА редуктазы рекомендованы для коррекции дислипидемии, но с учетом повышенного гепатотоксического риска их применения. Однако, для специфического лечения НАСГ применять ингибиторы ГМК-КоА редуктазы не рекомендуется
- – На фоне лечения ингибиторами ГМК-КоА редуктазы рекомендуется активный мониторинг каждые 3-4 нед в течение первых месяцев терапии:
- – определение сывороточных печеночных тестов (исследование уровня общего билирубина в крови, определение активности аспартатаминотрансферазы аланинаминотрансферазы, гамма-глютамилтрансферазы, щелочной фосфатазы в крови);
- – определение показателей углеводного и липидного обменов (исследование уровня глюкозы, триглицеридов, холестерина, холестерина липопротеинов низкой плотности, холестерина липопротеинов высокой плотности, инсулина в крови)
- – Рекомендован прием #урсодезоксихолевой кислоты** на фоне приема ингибиторов ГМК-КоА редуктазы в целях предупреждения развития цитолиза и повышения эффективности снижения повышенного уровня трансаминаз. Прием #уродезоксихолевой кислоты** (УДХК) в дозе 10-15 мг/кг/сут на фоне приема ингибиторов ГМК-КоА редуктазы сопровождается более выраженным снижением уровня ХС ЛПНП и рекомендуется для применения в реальной клинической практике
Комментарии: Комбинированное применение ингибиторов ГМК-КоА редуктазы и УДХК** предупреждает развитие цитолиза и способствует снижению повышенного уровня трансаминаз [76].
- – Кроме ингибиторов ГМК-КоА редуктазы при нарушении липидного обмена у пациентов НАЖБП рекомендованы как препараты выбора: фибраты, #никотиновая кислота, однако в настоящее время отсутствует достаточное количество РКИ по использованию их у пациентов с НАЖБП [35, 194, 213].
Комментарии: Режим дозирования #никотиновой кислоты – один раз в день перед сном в возрастающих дозах 375 мг, 500 мг и 750 мг (каждый в течение 1 недели), затем 1000 мг и 1500 мг (каждый в течение 4 недель) и далее 2000 мг (в течение 12 недель) [213].
В клиническом исследовании, включающем 186 пациентов с МС и НАЖБП, верифицированным по данным ультразвукового исследования, проводилась оценка влияния фенофибрата** на биохимические показатели липидограммы [212]. Пациенты были рандомизированы по монотерапии аторвастатином** в дозе 20 мг в сутки, фенофибрата** 200 мг в сутки и их комбинацию. Длительность исследования составила 54 недели. В исходе лечения отмечено статистически значимое снижение показателей уровней триглицеридов, общего холестерина, холестерина липопротеинов низкой плотности, а также повышение холестерина липопротеинов высокой плотности во всех трех группах пациентов, максимально выраженное при приеме фенофибрата в сочетании с аторвастатином [212]. В исследовании у 46 китайских пациентов с НАЖБП и дислипидемией (преимущественно с гипертриглицеридемий) при проведении оценки влияния #никотиновой кислоты пролонгированного действия на выраженность стеатоза печени, назначаемой в возрастающих дозах от 375 мг до 2000 мг в сутки в течение 12 недель, показано статистически значимое влияние препарата по снижению уровня триглицеридов сыворотки крови (-34,9 +/- 37, 6%) [213]. Следует отметить, что 7 пациентов прекратили прием препарата в связи с появлением побочных явлений в виде приливов жара и сыпи [213].
Медикаментозная терапия НАЖБП
Препараты для лечения заболеваний печени и желчевыводящих путей, обладающие гепатопротекторным действием (далее – Гепатопротекторы)
Для снижения выраженности повреждения печени (окислительного стресса воспаления, фиброзообразования) применяются препараты для лечения заболеваний печени и желчевыводящих путей, обладающие гепатопротекторным действием (далее -гепатопротекторы), способные воздействовать на звенья патогенеза НАЖБП.
Препараты для лечения заболеваний печени и желчевыводящих путей, обладающие гепатопротекторным действием (Гепатопротектор) – лекарственное средство, предотвращающее или ослабляющее клинико-функциональные и морфологические последствия токсико-метаболических повреждений печени
Клинические эффекты гепатопротекторов делятся на локальные и плейотропные:
Локальные:
- 1. Антистеатозный
- 2. Противовоспалительный
- 3. Антиоксидантный
- 4. Антифибротический
- 5. Антихолестатический
- 6. Регенераторный
- 7. Прочие
Плейотропные:
- 1. Холеретический
- 2. Гипоаммониемийный
- 3. Гиполипидемический
- 4. Нейротропный
- 5. Антиастенический
- 6. Системный цитопротективный
- 7. Антиинсулинорезистентный
- 8. Прочие
Предложенная классификация рандомизирует локальные и плейотропные эффекты гепатопротекторов, что в ситуации НАЖБП-коморбидности позволяет врачу выбрать наиболее рациональную моно- или комбинированную терапию с учетом не только прямых, но и побочных (нежелательных) эффектов каждого препарата.
Монопрепараты –
#Альфа-токоферола ацетат
- – #Альфа-токоферола ацетат в суточной дозе 800 ME у пациентов с НАЖБП, не имеющих СД, улучшает гистологическую картину печени и рекомендован как средство терапии первой линии в качестве антиоксиданта при лечении пациентов с доказанным НАСГ и прогрессирующим фиброзом (F2 и более)
Комментарии: альфа-токоферола ацетат является универсальным протектором клеточных мембран от окислительного повреждения, защищает биомембраны от их перекисной деструкции. Мембраностабилизирующее действие витамина проявляется и в его свойстве предохранять от окисления SH-группы мембранных белков. Альфа-токоферола ацетат является антигипоксантом, стабилизирующим митохондриальную мембрану и экономящим потребление клетками кислорода.
#Альфа-токоферола ацетат в суточной дозе 800 ME у пациентов с НАЖБП, не страдающих СД, позволяет снизить выраженность стеатоза и балонной дистрофии и стимулировать регресс НАСГ [77, 78]. В исследовании PIVENS применение альфа-токоферола ацетата (800 ME в сутки) позволило снизить выраженность стеатоза, воспаления и баллонной дистрофии и стимулировать регресс НАСГ у 36% пациентов (21% в группе плацебо) [77]. В долгосрочном исследовании (средний период наблюдения составил 5,6 лет) прием альфа-токоферола ацетата в дозе 800 ME 2 и более у пациентов с продвинутыми стадиями НАЖБП 800 ME >= 2 лет снизил риск смерти или потребность в трансплантации и печеночной декомпенсации без влияния на развитие гепатоцеллюлярной карциномы и ССС. 10-летняя кумулятивная вероятность гепатоцеллюлярной карциномы, сосудистых событий и непеченочного рака не различалась [79].
Высокие дозы альфа-токоферола ацетата (более 800 мг в сутки) при длительном приеме могут оказывать проканцерогенный эффект в отношении рака предстательной железы и увеличивают риск смерти от всех причин [77], поэтому вопрос об их использовании должен решаться в качестве персонализированного решения. Витамин E в больших количествах содержится в растительных маслах из пшеничных зародышей, подсолнуха, оливок, кукурузы, тыквы, хлопка, льна и сои. Для сохранения полезных качеств продукта в кулинарных целях лучше применять эти масла в качестве составляющей салатов. Витамин E содержится также в семечках, орехах, горохе, фасоли, семенах льна, овсе, печени, желтках, молоке, зеленых листовых овощах.
- – Назначение альфа-токоферола ацетата не рекомендовано при сочетании НАЖБП и СД, при НАЖБП без НАСГ и фиброза, при подозрении на НАСГ, но без гистологического подтверждения, а также при исходе НАЖБП в ЦП [2, 33, 36].
#Урсодезоксихолевая кислота** (УДХК)
- – #УДХК** в дозе 10-15 мг/кг/сутки в 2 приема в течение не менее года, иногда до 2-х лет и более, рекомендована:
- – при всех формах НАЖБП, особенно с признаками вне- и внутрипеченочного холестаза, сердечно-сосудистой патологией;
- – для лечения пациентов с признаками НАСГ [195].
Комментарии: УДХК** – желчная кислота, оказывающая прямое гепатопротекторное действие и уменьшающая гепатотоксичность гидрофобных солей желчи. Молекула обладает метаболическим и плейотропным действием, оказывает влияние на энтерогепатическую циркуляцию желчных солей, уменьшая реабсорбцию в кишечнике эндогенных более гидрофобных и потенциально токсичных соединений, а также воздействует на фарнезиодные рецепторы, оказывая антифибротические действие [80]. УДХК** уменьшает выраженность стеатоза печени по данным неинвазивных методов исследования [81-84], высокие дозы УДХК** уменьшают выраженность балонной дистрофии [85]. УДХК** снижает содержание холестерина в желчи преимущественно путем дисперсии холестерина и формирования жидко-кристаллической фазы [86]. УДХК** снижает литогенный индекс желчи, увеличивая содержание в ней желчных кислот, способствует частичному или полному растворению холестериновых желчных камней при пероральном применении, оказывает холеретическое действие [87]. Помимо этого, желчные кислоты (ЖК) действуют как метаболически активные сигнальные молекулы, контролирующие печеночный липогенез de novo, экспорт липопротеинов очень низкой плотности, участвуют в регуляции глюконеогенеза в печени, синтеза гликогена и чувствительности к инсулину [76, 88, 89].
Результаты отечественного многоцентрового исследования “УСПЕХ” также показали, что УДХК** улучшает показатели липидного обмена и обладает потенциальными антиатерогенными свойствами. У женщин также достоверно снизился показатель толщины интима-медиа каротидных артерий ТКИМ и десятилетний риск сердечно-сосудистых осложнений по калькулятору ASCVD 2013 [84].
#Фосфолипиды (ФЛ)
- – #ФЛ как препараты выбора рекомендуются для лечения пациентов с признаками стеатоза печени вне зависимости от стадии заболевания (НАЖБП/НАСГ) [91-
Комментарии: Эффективность ФЛ в терапии заболеваний печени реализуется за счет способности 3-sn-фосфатидилхолина (основное действующее вещество) включаться в поврежденные участки мембран гепатоцитов. ФЛ также способны конкурентно замещать эндогенные фосфолипиды с меньшим количеством полиненасыщенных жирных кислот, что увеличивает пластичность мембран и улучшает их функционирование, стабилизируют мембраны, обладают антиоксидантным, цитопротективным и противовоспалительным действием [90]. Пероральная форма ФЛ приводила к значимому регрессу стеатоза у пациентов с НАЖБП/НАСГ по данным биопсии печени, УЗИ и КТ в 7 рандомизированных контролируемых исследованиях – отмечается стабильно высокая амплитуда и гомогенность эффекта [91-97]. Также в данных исследованиях показано значимое снижение трансаминаз (АЛТ, АСТ, ГГТ) и липидного профиля. Имеются данные в отношении замедления процесса фиброзирования при длительном применении препарата у пациентов с НАЖБП [96]. Систематический обзор и метаанализ, подтвердил регресс стеатоза при терапии ФЛ в РКИ, а также положительное влияние на трансаминазы и липидный профиль у пациентов с НАЖБП/НАСГ [98]. В наблюдательном исследовании MANPOWER 2018, включающим 2843 пациента со стеатозом печени и кардиометаболической коморбидностью, продемонстрировано улучшение УЗИ картины у 69,6% пациентов после трехмесячного приема препарата и у 81,4% пациентов через 6 месяцев терапии [99]. Прием ФЛ осуществляется в дозе 1800 мг/сутки, курсами по 3-6 месяцев – 2-3 раза в год [99].
- – ФЛ рекомендованы у пациентов с НАЖБП и сопутствующей сердечно-сосудистой и/или метаболической патологией (артериальная гипертензия, сахарный диабет 2 типа, дислипидемия, ожирение) в качестве дополнительной терапии [99].
Комментарии: В зависимости от соотношения количеств линолевой и линоленовой кислот у препаратов ЭФЛ могут отмечаться дополнительные гиполипидемические свойства, анализ результатов исследования MANPOWER продемонстрировал дополнительные гиполипидемические возможности при назначении ЭФЛ на 12 и 24 недели пациентам с НАЖБП [99].
Адеметионин**
- – Адеметионин** как препарат выбора рекомендован для лечения пациентов с НАЖБП [100].
Комментарии: S-адеметионин-L-метионин участвует в трех основных типах биохимических реакций: трансметилирование, транссульфирирование и аминопропилирование [100, 101]. Эта молекула является основным донором метильных групп в реакциях синтеза аминокислот, фосфолипидов, гистонов, биогенных аминов и белков [102]. S-адеметионин – универсальный антиоксидант, кроме того, он является предшественником синтеза глютатиона [103, 104]. Убедительных данных о клинически значимом долгосрочном положительном влиянии Адеметионина** на биохимическую и гистологическую картину при НАСГ не получено. Адеметионин** также рекомендован пациентам с НАЖБП при выявлении у них синдрома внутрипеченочного холестаза [100].
Мультицентровое наблюдательное исследование 250 пациентов с НАЖБП и проявлениями внутрипеченого холестаза продемонстрировало, что 6-ти недельный прием Адеметионина** сопровождался значимым снижением симптомов внутрипеченочного холестаза (желтухи, зуда кожи, лабораторных маркеров холестаза), а также снижением количества дней нетрудоспособности и посещений врачей [105].
- – Адеметионин** рекомендован пациентам с НАЖБП при наличии повышенной утомляемости (т.н. “циркадный синдром”), а также при сочетании НАЖБП и алкогольного поражения печени [100].
Комментарии: У пациентов с хроническими заболеваниями печени S-адеметионин-L-метионин оказывает дополнительное противоастеническое действие [106-111]. Метаанализ, включающий 25 контролируемых исследований свидетельствует, что эффективность S-адеметионина как антидепресанта существенно превышает эффект плацебо и сопоставима с трициклическими антидепрессантами [112].
Орнитин
- – Орнитин рекомендован в дозе 6-9 г/сутки перорально для лечения пациентов с НАЖБП и гипераммониемией до нормализации показателей уровней аммиака-аммония, а также регрессии проявлений печеночной энцефалопатии по тесту связи чисел (ТСЧ) (Приложение Г15) [196].
Комментарии: Орнитин – это смесь эндогенных аминокислот с доказанной способностью усиливать выведение аммиака при паренхиматозных повреждениях печени [113]. Показана возможность дозозависимого эффекта на выраженность стеатоза печени у пациентов с НАЖБП [114], а у пациентов с НАСГ значительно улучшались показатели КТ соотношения печень/селезенка [115]. Продемонстрирована возможность Орнитина влиять на печеночную микроциркуляцию, улучшение зарегистрировано в том числе и при наличии фиброза 0-1 стадии [116]. Главный механизм действия Орнитина, который лежит в основе его свойств в качестве детоксиканта аммиака при хроническом заболевании печени, включает выведение аммиака двумя различными путями, а именно интенсификацией синтеза мочевины перипортальными гепатоцитами (L-орнитин является промежуточным продуктом метаболизма в цикле образования мочевины) и синтеза глутамина с помощью фермента глутаминсинтетазы (GS), локализованного и перивенозных гепатоцитах, и в скелетных мышцах. Механизмы обеспечения благоприятного действия Орнитина при НАЖБП осуществляется через механизмы метаболические трансформации L-орнитина и L-аспартата в L-глутамин, L-аргинин и глутатион. Эффект заключается в предотвращении перекисного окисления липидов, улучшении печеночной микроциркуляции, противовоспалительном и антиоксидантном действии [117]. Российский консенсус “Гипераммониемии у взрослых” рекомендует использовать этот препарат в парентеральной и энтеральной формах у пациентов с гепатаргенной гипераммониемией и различными стадиями печеночной энцефалопатии, а также для снижения рисков прогрессирования патологии печени на фоне гипераммониемии [118].
Расторопши пятнистой плодов экстракт
- – Расторопши пятнистой плодов экстракт как препарат выбора рекомендован для лечения пациентов с признаками НАЖБП-стеатоза печени и стеатогепатита, особенно при сопутствующих токсических и лекарственных поражениях печени
Комментарии: Данные о влиянии Расторопши пятнистой плодов экстракт на пациентов с НАЖБП ограничены. Однако некоторые исследования показали, что лечение Расторопши пятнистой плодов экстрактом было связано с улучшением окислительного профиля из -за способности силимарина подавлять выработку провоспалительных цитокинов [119]. Показано снижение выраженности стеатоза печени при использовании комбинации диеты, препарата расторопши пятнистой и альфа-токоферола ацетата [120]. По сравнению с плацебо, лечение Расторопши пятнистой плодов экстрактом в дозе 700 мг 3 раза в день в течение 48 недель значительно улучшило показатели подтвержденные данными биопсии признаки фиброза у 99 пациентов с НАСГ и НАС >= 4 [121]. В плацебо-контролируемом исследовании у 100 пациентов с неалкогольным стеатогепатитом (силимарин назначался в дозе 280 мг на протяжении 24 недель) в 52% случаев отмечена нормализация АЛТ (в группе плацебо-18%, p = 0,001). Статистически значимое снижение АСТ до нормального уровня отмечено у 62% пациентов vs 20% в группе плацебо, p < 0,0001 [122]. Курсы лечения Расторопши пятнистой плодов экстрактом не стандартизованы и рассчитаны на длительный временной период.
#Таурин
- – #Таурин как препарат выбора рекомендован в дозе 1000 мг/сутки, курсами по 3 месяца 2-3 раза в год:
- – для лечения пациентов с НАЖБП при сердечно-сосудистой коморбидности;
- – для лечения пациентов с признаками НАСГ;
- – в лечении пациентов с НАЖБП и сахарным диабетом 1 и 2 типа, метаболическом синдроме, ишемической болезни сердца [199-201].
Комментарии: Таурин (2-аминоэтансульфоновая кислота) – наиболее распространенная свободная аминокислота в организме человека, образуется в гепатоцитах в результате обмена веществ из метионина и цистеина через гипотаурин. В печени таурин играет важную роль в метаболизме желчи, модулируя уровни холестерина в крови, и образует конъюгаты с желчными кислотами (главным образом, холевой и дезоксихолевой) с образованием желчной соли таурохолата – главной соли желчи, которая составляет основной путь выведения холестерина из плазмы. Таурин также активирует ХС-7a-гидроксилазу, ограничивающую скорость фермента, участвующего в синтезе желчной кислоты из холестерина [126, 127]. Оказывает антиоксидантное, антиапоптотическое и противовоспалительное действие [128]. Дефицит таурина является одним из важных патогенетических механизмов, участвующих в формировании дисфункции висцерального жира, прогрессирования НАЖБП. Продемонстрировано достоверное влияние таурина на выраженность стеатоза и фиброза печени у пациентов с НАЖБП [129-132]. Помимо гепатопротективного действия, таурин является физиологическим ингибитором ренин-ангиотензин-альдостероновой системы, что обуславливает его положительные кардиотропные эффекты [133, 134]. Дополнительные гипогликемизирующие и гиполипидемические возможности таурина обуславливает включение в показания к применению этого препарата – сахарного диабета 1 и 2 типа, гиперхолестеринемию [135-137].
#Лаеннек
- – #Лаеннек как препарат выбора рекомендован для лечения пациентов с НАЖБП/НАСГ и гиперферритинемией. Препарат вводится парентерально, по 4,0 мл в/в в 250 мл физ. р-ра, либо при невозможности внутривенного введения – внутримышечно по 4,0 мл через день, курс 20 процедур. Между курсами назначается поддерживающая терапия: 1 раз в 10 дней по 6,0 мл от 3 до 7 мес
Комментарии: Лаеннек для парентерального введения имеет выраженные иммуномодулирующие и гепатопротекторные свойства. Биологически активные вещества гидролизата (факторы роста гепатоцитов, инсулиноподобный и др. факторы роста, противовоспалительные интерлейкины) стимулируют регенерацию гепатоцитов, проявляют дезинтоксикационные свойства, активируют обмен веществ в печени, снижают отложение холестерина и липидов в печеночных клетках, повышают активность тканевого дыхания, снижают интенсивность развития соединительной ткани в печени. У пациентов с НАЖБП Лаеннек оказывает противовоспалительное, антиоксидантное действие, уменьшает проявления инсулинорезистентности, способствует нормализации функции печени, показателей липидного обмена и таким образом нормализует дистрофические, воспалительно-некротические, фибротические процессы в печени. Курсовая терапия гидролизатом плаценты человека показана при повышении уровня ферритина [138].
#Морфолиний-метил-триазолил-тиоацетат
– #Морфолиний-метил-триазолил-тиоацетат как препарат выбора рекомендован для лечения пациентов с НАЖБП и сердечно-сосудистой коморбидностью. Лечение проводится в два этапа: на первом этапе препарат вводится парентерально, в/в капельно 100 мг (4 мл), курс 5 дней; затем в таблетированной форме 600 мг в сутки (200 мг x 3 раза в день) в течение 14 дней
Комментарии: Морфолиний-метил-триазолил-тиоацетат оказывает атиоксидантное действие: в его структуре присутствует тиольная группа, за счет которой препарат имеет выраженную восстанавливающую способность и является акцептором электронов от нестойкой активной формы кислорода, обладает мембраностабилизирующим эффектом, который обусловлен его антиоксидантными свойствами. Препарат активирует лактатдегидрогеназу и пируваткиназу, ферменты малат-аспартатного челночного механизма, что активизирует аэробный и анаэробный пути окисления глюкозы, вследствие чего восстанавливается макроэргический пул и снижается лактат-ацидоз в гепатоцитах даже при развитии гипоксии [139, 140]. Оказывает дополнительное антиангинальное действие, что может быть использовано у пациентов с НАЖБП и ИБС [141-143]. В исследовании программы ТРИГОН-1 “Терапевтическая эффективность монотерапии тиотриазолином у пациентов с НАЖБП и сердечно-сосудистыми рисками”, целью которого являлось изучение механизмов формирования коморбидности у пациентов с неалкогольными стеатогепатозами и предикторами сердечно-сосудистых заболеваний и влияния на них полиорганной терапии, было показано, что прием препарата морфолиний-метил-триазолил-тиоацетат с полиотропным действием у пациентов с НАЖБП улучшает состояние печени и снижает риски ССЗ [144].
Коррекция нарушений функции желчевыводящих путей при НАЖБП
#Артишока листьев экстракт
- – #Артишока листьев экстракт в составе экстракта из листьев артишока рекомендован в дозе 400 мг 3 раза в день в течение 4 недель пациентам с НАЖБП при наличии патологии желчевыводящих путей
Комментарии: Флавоноид цинарин является основным компонентом препарата растительного происхождения из листьев артишока полевого. Экстракт из листьев артишока полевого содержит различные растительные компоненты, оказывающие противовоспалительное действие и уменьшающие литогенность желчи. Цинарин в сочетании с фенолокислотами обладает желчегонным, а также гепатопротекторным действием. При курсовом лечении экстракт артишока улучшает холерез и холекинез, улучшает реологические свойства желчи, способствует раскрытию сфинктера Одди и устраняет билиарный сладж [145-148].
- – #Артишока листьев экстракт в дозе 400 мг 3 раза в сутки в течение 3 месяцев рекомендован для достижения целевых уровней холестерина и триглицеридов на фоне лечения низкими дозами статинов у пациентов с НАЖБП
Комментарии: Экстракт листьев артишока оказывает плейотропное действие: гепатопротективный, гиполипидемический, антиоксидантный, дезинтоксикационный, холеретический, холекинетический, диуретический, гипоазотемический, пребиотический и др. [149, 150, 151]. Плейотропное действие артишока было продемонстрировано в работе W. Englisch, C. Beckers и соавт. в 2000 г. [152]. В исследовании приняли участие 143 пациента с начальным уровнем общего ХС (ОХС) > 7,3 ммоль/л, в течение 6 нед принимавшие 1800 мг сухого экстракта артишока или плацебо. Уменьшение ОХС в группе комбинированной терапии составило 19% по сравнению с 8,6% в группе плацебо. Уровень ХС ЛПНП в группе артишока снизился на 22,9%, в группе плацебо – на 6,3%. Соотношение ЛПНП/ЛПВП уменьшилось на 20,2% в группе артишока и на 7,2% – в группе плацебо. Позднее в двойном слепом плацебо-контролируемом исследовании R. Bundy с участием 131 пациента с уровнем ХС 6-8 ммоль/л экстракт листьев артишока также показал свою эффективность [153]. Основная группа получала суточную дозу артишока 1280 мг в течение 12 нед, в результате чего уровень ХС плазмы в основной группе снизился в среднем на 4,2% по сравнению с группой плацебо, в которой уровень ХС увеличился на 1,9%. В двойном слепом плацебо -контролируемом исследовании В. Рангбу 60 пациентов с НАСГ принимали артишок (Cynara scolymus) по 6 таблеток в день в течение 12 нед. [154]. На фоне терапии наблюдалось значимое снижение ОХС, ЛПНП и ТГ по сравнению с группой плацебо [152-154]. Полученные результаты согласуются с данными других исследователей. В открытом сравнительном исследовании (n = 60) было показано, что экстракт из листьев артишока полевого оптимизирует схему терапии НАЖБП статинами: повышение дозы статинов до 20 мг по эффективности сопоставимо с комбинированной терапией статинами в дозе 10 мг в сочетании с экстрактом из листьев артишока полевого по 2 таблетки (200 мг) 3 раза в день в течение 3 мес. [155]. В подгруппе пациентов, получавших комбинированную терапию Экстракта из листьев артишока полевого + статины в дозе 10 мг, не отмечалось повышения уровня печеночных трансаминаз, что свидетельствует об отсутствии токсической нагрузки на печень. Экстракт из листьев артишока полевого может быть показан для достижения целевых уровней ХС и ТГ на фоне лечения низкими дозами статинов у пациентов с НАЖБП. Подобная комбинированная гиполипидемическая терапия позволяет обойтись без повышения дозы статинов, что предотвращает прогрессирование НАЖБП, а также способствует снижению рисков развития сердечно-сосудистых осложнений [155-158].
Комбинированное применение гепатопротекторов
- – С целью достижения максимальной эффективности и безопасности при лечении пациентов с НАЖБП-коморбидностью при принятии решения о назначении комбинированной гепатопротекторной терапии рекомендовано:
- – руководствоваться положениями Приложения А3.1;
- – четко сформулировать целевые промежуточные и конечные точки эффективности лечения;
- – использовать принципы многоцелевой (мультитаргентной) монотерапии и рационального комбинирования;
- – исключить иррациональные комбинации, полипрагмазию и возможность развития нежелательных (побочных) эффектов [2, 33].
Официнальные комбинации
Глицирризиновая кислота + Фосфолипиды**
Пациентам с НАЖБП Глицирризиновая кислота + Фосфолипиды** рекомендован как препарат выбора
Комментарии: Теоретическим обоснованием эффективности фиксированной
комбинации Глицирризиновая кислота + Фосфолипиды** является способность глицирризиновой кислоты (ГК) защищать фосфолипиды от окисления, а фосфолипидов – повышать липофильность ГК, способствуя увеличению ее биодоступности. Клиническая эффективность комбинации показана в небольшом количестве отечественных исследований [159, 160, 161, 162]. 45 пациентов с НАСГ и артериальной гипертонией, сахарным диабетом и дислипидемией первые 10 дней получали внутривенно по 400 мг/сут в пересчете на ГК; затем – per os по 70 мг ГК 3 р/сут в течение 60 дней. Нормализация активности АЛТ, АСТ, ГГТ и статистически более значимое уменьшение размеров печени по данным ультразвукового исследования отмечалась у достоверно большего числа пациентов, нежели в контрольной группе. На фоне введения комбинированного препарата ГК отмечались единичные обратимые, слабо выраженные побочные явления: кожная сыпь, зуд, диспепсические явления, при внутривенном введении было отмечено 2 случая умеренного повышения артериального давления [161]. В двойное слепое плацебо-контролируемое исследование были включены 180 пациентов с НАЖБП. Комбинированный препарат ГК в дозе по ГК – 400 мг/сут вводился внутривенно в течение 10 дней, затем в течение 10 недель пациенты принимали таблетки в дозе по 70 мг 3 р/сут перорально. Контрольная группа получала плацебо по той же схеме в аналогичных лекарственных формах. После завершения лечебного курса уровень адипонектина у пациентов основной группы повышался статистически более значимо, одновременно сопровождаясь отрицательной динамикой индекса фиброза печени (по шкале NAFLD fibrosis score). Профиль безопасности двух режимов терапии оказался сопоставимыми [162].
- – #Инозин + Меглумин + Метионин + Никотинамид + Янтарная кислота в растворе в виде фиксированной комбинации 400 мл внутривенно капельно со скоростью введения 40-60 капель в минуту, 1 раз в сутки (утром), ежедневно в течение 10 дней рекомендуется как средство инициальной терапии у пациентов с НАЖБП в стадии стеатогепатита [163].
Комментарии: Включение этого препарата в схему лечения пациентов с НАЖБП на стадии стеатогепатита достоверно повышало эффективность лечения, выражающееся в более быстром купировании астеновегетативного и диспепсического синдромов, и уменьшении выраженности биохимических проявлений цитолитического и холестатического синдромов
Продукция для печени от компании Сово-Сова
ТАУХОЛ — при жировой болезни печени
- растворяет и выводит жир из печени;
- способствует окислению свободных жирных кислот;
- снижает липогенез;
- изменяет соотношение потребления энергии для синтеза гликогена и липогенеза печени;
- снижает холестерин крови;
- снижает секрецию липопротеинов низкой плотности из печени;
- увеличивает выведение холестерина из крови;
- способствует связыванию холестерина с желчными кислотами;
- способствует выделению желчных кислот с калом;
- подавляет всасывание желчных кислот в подвздошной кишке;
- растворяет и выводит жир из печени;
- оказывает гипогликемический эффект при сахарном диабете 2 типа;
- способствует работе бета-клеток поджелудочной железы;
- способствует секреции инсулина;
- снижает инсулинорезистентность;
- оказывает антиоксидантный эффект;
- оказывает противовоспалительный эффект;
- влияет на обмен желчных кислот;
- проявляет гипотензивный эффект;
- ингибирует ренин-ангиотензин- альдостероновую систему;
- стимулирует калликреин- кининовую систему;
- оказывает вазорелаксирующий эффект.
Печенол (КАПСУЛЫ) – защита и укрепление состояния печени.
Хирургическое лечение НАЖБП
- – При отсутствии эффекта от немедикаментозных мероприятий и адекватной медикаментозной терапии у лиц с ожирением рекомендовано рассмотреть вопрос о проведении хирургического бариатрического лечения
Комментарии: кандидатами для хирургического вмешательства являются пациенты с выраженным морбидным ожирением при отсутствии возможности других способов снижения веса.
- – Пациентам с НАЖБП и декомпенсированным циррозом печени либо формированием ГЦК рекомендовано рассмотреть возможность проведения трансплантации печени [36].
Комментарии: трансплантация печени является наиболее эффективным и часто единственным радикальным методом лечения пациентов с терминальной стадией НАЖБП и злокачественными опухолями печени, позволяет увеличить продолжительность жизни пациентам с декомпенсированным ЦП и ГЦК. Вопрос о показаниях к ее проведению и постановке пациентов в лист ожидания трансплантации печени должен решаться в соответствии с действующими клиническими рекомендациями.
Другие методы лечения
Коррекция дисбиоза
При выявлении у пациента с НАЖБП печеночной энцефалопатии, в патогенетическую терапию рекомендуется включать рифаксимин в дозе 400 мг три раза в день
Комментарии: Подавление уреазапродуцирующей кишечной микрофлоры является одним из компонентов устранения причин гипераммониемии и, соответственно, печеночной энцефалопатии, в том числе латентной. Снижение выраженности печеночной энцефалопатии у пациентов с ЦП на фоне применения рифаксимина доказано в РКИ и метаанализе
- – При принятии решения о выборе биотической терапии пациентам с НАЖБП и признаками дисбиоза рекомендовано руководствоваться рекомендациями Всемирной гастроэнтерологической организации (ВГО)
Комментарии: ВГО рекомендует при НАЖБП/НАСГ следующие мультиштаммовые пробиотические продукты:
при НАЖБП:
- – Йогурт (с Lactobacillus bulgaricus и Streptococcus thermophilus) обогащенный L. acidophilus La5 и Bifidobacterium lactis Bb12 300 г ежедневно, показатель эффективности – снижение уровня трансаминаз;
- – Смесь Lactobacillus casei, L. rhamnosus, Streptococcus thermophilus, Bifidobacterium breve, L. acidophilus, B. longum и L. bulgaricus + фруктоолигосахариды, минимум 107 КОЕ дважды в день, показатели эффективности – снижение уровня трансаминаз, улучшение индекса инсулинорезистентности (индекс HOMA IR) и данных транзиентной эластрографии;
при НАСГ:
- – Lactobacillus bulgaricus и Streptococcus thermophiles, таблетка 500 миллионов, один раз в день, показатель эффективности – снижение уровня трансаминаз;
- – Bifidobacterium longum W11 + FOS 5,000 миллионов живых бактерий один раз в день, показатели эффективности – снижение уровня трансаминаз и выраженности воспаления показателей по шкале гистологической активности НАСГ [170].
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.